दैनिक जीवन में रसायन विज्ञान विषय विज्ञान और प्रौद्योगिकी का एक महत्वपूर्ण भाग है। हमारे दैनिक जीवन में उपयोग होने वाले साबुन, दवाइयाँ, खाद्य पदार्थ, सौंदर्य प्रसाधन तथा ईंधन आदि में रसायन विज्ञान का महत्वपूर्ण योगदान है। रसायन विज्ञान के कारण मानव जीवन अधिक सुविधाजनक, सुरक्षित और आधुनिक बना है।
- कटे हुए सेब का रंग कुछ समय बाद भूरा हो जाता है। क्योंकि पॉलीफेनॉल ऑक्सीडेज नामक एंजाइम, सेब में मौजूद फिनोलिक यौगिकों का एंजाइमीय ऑक्सीकरण कर देता है।
- प्याज काटते समय आंखों से पानी आने लगता है। इसका कारण है – प्याज से निकलने वाली सल्फर-आधारित वाष्पशील गैस आँसुओं के संपर्क में आकर हल्का सल्फ्यूरिक अम्ल बना देती है।
- दूध से दही बनने की प्रक्रिया में लैक्टोबैसिलस नामक जीवाणु महत्वपूर्ण भूमिका निभाते हैं। ये जीवाणु दूध में मौजूद लैक्टोज का किण्वन करके उसे लैक्टिक अम्ल में बदल देते हैं, जिससे दूध का प्रोटीन केसीन जम जाता है और दही बन जाता है।
- ब्रेड या रोटी के फूलने का कारण खमीर (यीस्ट) है। किण्वन की प्रक्रिया के दौरान खमीर कार्बन डाइऑक्साइड गैस उत्पन्न करता है, जो आटे में भर जाती है और आटा फूल जाता है।
- बुलेटप्रूफ काँच जिसे बैलिस्टिक ग्लास भी कहा जाता है, काँच की कई परतों को मजबूत पदार्थों की परतों के साथ जोड़कर बनाया जाता है। इन परतों के बीच सामान्यतः उच्च-मजबूती वाला विनाइल प्लास्टिक, जैसे पॉलीविनाइल ब्यूटिरल लगाया जाता है, जो टकराव की ऊर्जा को अवशोषित कर लेता है।
- बुलेटप्रूफ जैकेट बनाने में केवलर का उपयोग किया जाता है।
- इमारतों में उपयोग होने वाले अग्निशामक यंत्र में कार्बन डाइऑक्साइड भरी होती है।
- मतदान के बाद उंगली पर लगाई जाने वाली अमिट स्याही में सिल्वर नाइट्रेट होता है।
- एलपीजी सिलेंडर से गैस के रिसाव के समय आने वाली तेज दुर्गंध एथिल मरकैप्टन के कारण होती है।
- गोताखोर कृत्रिम श्वसन के लिए गैस सिलेंडरों में ऑक्सीजन और हीलियम के मिश्रण का उपयोग करते हैं।
पदार्थ और उसकी प्रकृति
- पदार्थ : संसार की कोई भी वस्तु जो स्थान घेरती है, द्रव्यमान रखती है और जिसकी संरचना में परिवर्तन हो सकता है, उसे पदार्थ कहते हैं। उदाहरण—पानी, वायु, रेत आदि।
- प्राचीन समय में भारतीय और यूनानी विद्वानों का मानना था कि प्रकृति की सभी वस्तुएँ पाँच तत्वों के मेल से बनी हैं। ये पाँच तत्व हैं—आकाश, जल, पृथ्वी, अग्नि और वायु।
पदार्थ का वर्गीकरण
- ठोस : पदार्थ की वह अवस्था जिसमें आकार और आयतन दोनों निश्चित होते हैं, उसे ठोस कहते हैं। उदाहरण—पत्थर, लकड़ी, काँच की चूड़ियाँ, बर्फ के टुकड़े आदि।
- द्रव : पदार्थ की वह अवस्था जिसमें आकार निश्चित नहीं होता लेकिन आयतन निश्चित होता है, उसे द्रव कहते हैं। उदाहरण—अल्कोहल, पानी, तारपीन का तेल, खाद्य तेल आदि।
- गैस : पदार्थ की वह अवस्था जिसमें आकार और आयतन दोनों निश्चित नहीं होते, उसे गैस कहते हैं। उदाहरण—वायु, ऑक्सीजन आदि।
- नोट : गैस की कोई मुक्त सतह नहीं होती। इसका प्रसार बहुत अधिक होता है और इसे आसानी से संपीड़ित किया जा सकता है।
- पदार्थ की चौथी अवस्था को प्लाज्मा कहा जाता है।
- पदार्थ की पाँचवीं अवस्था को बोस–आइंस्टीन संघनन (बोस-आइंस्टीन कंडेनसेट) कहा जाता है।
तत्व
- तत्व वह शुद्ध पदार्थ है जिसे किसी ज्ञात भौतिक या रासायनिक विधि द्वारा दो या अधिक पदार्थों में विभाजित नहीं किया जा सकता, और न ही इसे अन्य सरल पदार्थों के संयोजन से बनाया जा सकता है।
- उदाहरण—सोना, चाँदी, ऑक्सीजन आदि।
यौगिक
- यौगिक वह शुद्ध पदार्थ है जो दो या दो से अधिक तत्वों के निश्चित अनुपात में रासायनिक संयोजन से बनता है। किसी यौगिक के गुण उसके बनने वाले तत्वों के गुणों से भिन्न होते हैं। उदाहरण—जल।
- जल ऑक्सीजन और हाइड्रोजन के संयोजन से बनता है। ऑक्सीजन दहन को सहारा देती है और हाइड्रोजन स्वयं जलती है, लेकिन इन दोनों से बना यौगिक जल आग को बुझा देता है।
मिश्रण
- मिश्रण वह पदार्थ है जो दो या दो से अधिक तत्वों या यौगिकों को किसी भी अनुपात में मिलाने से बनता है। इसे सरल यांत्रिक विधियों द्वारा उसके मूल घटकों में अलग किया जा सकता है। उदाहरण—वायु।
परमाणु संरचना
- परमाणु : परमाणु किसी तत्व का सबसे छोटा कण होता है जो रासायनिक अभिक्रिया में भाग ले सकता है।
- अणु : अणु किसी तत्व या यौगिक का सबसे छोटा कण होता है जो स्वतंत्र अवस्था में अस्तित्व में रह सकता है।
आधुनिक परमाणु सिद्धांत
- आधुनिक परमाणु सिद्धांत के जनक जॉन डाल्टन माने जाते हैं। डाल्टन के परमाणु सिद्धांत के अनुसार परमाणु आपस में सरल पूर्णांक अनुपात में मिलकर अणुओं का निर्माण करते हैं।
- 20वीं शताब्दी में जे. जे. थॉमसन, रदरफोर्ड और चैडविक आदि वैज्ञानिकों की आधुनिक खोजों से यह सिद्ध हुआ कि परमाणु तीन कणों से मिलकर बना होता है—इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन।
| कण | आवेश | द्रव्यमान (ग्राम) | खोजकर्ता |
| इलेक्ट्रॉन (e⁻) | –1 | 9.1095 × 10⁻²⁸ g | जे. जे. थॉमसन |
| प्रोटॉन (p⁺) | +1 | 1.6726 × 10⁻²⁴ g | गोल्डस्टीन |
| न्यूट्रॉन (n⁰) | 0 | 1.6749 × 10⁻²⁴ g | चैडविक (1932) |
नोट : –
- भारतीय वैज्ञानिक सत्येन्द्र नाथ बोस के नाम पर मूलभूत कण को बोसॉन कहा जाता है।
रदरफोर्ड का परमाणु का नाभिकीय मॉडल
- रदरफोर्ड ने अपने विद्यार्थियों हैंस गीगर और अर्नेस्ट मार्सडेन के साथ मिलकर एक बहुत पतली सोने की पन्नी पर अल्फा कणों की बौछार की और परमाणु का नाभिकीय मॉडल प्रस्तुत किया।
- रदरफोर्ड के मॉडल के अनुसार—
- परमाणु का धनात्मक आवेश और उसका अधिकांश द्रव्यमान परमाणु के एक अत्यंत छोटे क्षेत्र में केंद्रित होता है, जिसे नाभिक कहा जाता है।
- इलेक्ट्रॉन नाभिक के चारों ओर वृत्ताकार मार्गों में तेज गति से घूमते हैं।
- इलेक्ट्रॉन और नाभिक के बीच स्थिर वैद्युत स्थैतिक आकर्षण बल होता है।
- रदरफोर्ड मॉडल की सीमाएं
- यह मॉडल परमाणु की स्थिरता को स्पष्ट नहीं कर सका।
- यह मॉडल इलेक्ट्रॉनिक संरचना को नहीं समझा पाया, अर्थात यह नहीं बता सका कि इलेक्ट्रॉन नाभिक के चारों ओर किस प्रकार व्यवस्थित रहते हैं और उनकी ऊर्जा क्या होती है।
हाइजेनबर्ग का अनिश्चितता सिद्धांत
- इस सिद्धांत के अनुसार किसी कण की स्थिति और वेग को एक ही समय पर सटीक रूप से निर्धारित करना असंभव है।
बंध
- इलेक्ट्रॉनों के पुनर्वितरण के परिणामस्वरूप बनने वाले बंध को रासायनिक बंध कहते हैं।
- रासायनिक बंध तीन प्रकार के होते हैं—
- आयनिक बंध – जब इलेक्ट्रॉनों के स्थानांतरण से बंध बनता है, तो उसे आयनिक बंध कहते हैं। उदाहरण— Na⁺ : Cl⁻ → NaCl
- सहसंयोजक बंध –जब दो या अधिक परमाणु अपने संयोजक कक्ष के इलेक्ट्रॉनों को साझा करते हैं, तो उनके बीच बनने वाला स्थायी बंध सहसंयोजक बंध कहलाता है। उदाहरण— Cl : Cl → Cl₂
- उपसहसंयोजी बंध – जब दो परमाणुओं के बीच इलेक्ट्रॉन युग्म साझा होता है, लेकिन यह इलेक्ट्रॉन युग्म केवल एक ही परमाणु द्वारा दिया जाता है, तब बनने वाला बंध समन्वय बंध कहलाता है। उदाहरण— H₂SO₄ के निर्माण में सल्फर के चारों ओर दो समन्वय बंध पाए जाते हैं।
- हाइड्रोजन बंध
- हाइड्रोजन (H) का फ्लोरीन (F), ऑक्सीजन (O) या नाइट्रोजन (N) के साथ बनने वाले यौगिकों में हाइड्रोजन बंध पाया जाता है। उदाहरण— HF, H₂O, NH₃
- चूँकि हाइड्रोजन (H) विद्युत धनात्मक होता है और फ्लोरीन (F) अत्यधिक विद्युत ऋणात्मक होता है, इसलिए H और F के बीच बनने वाला सहसंयोजक बंध कमजोर हो जाता है और इनके बीच हाइड्रोजन बंध बनता है।
- हाइड्रोजन बंध एक कमजोर स्थिर वैद्युत आकर्षण बल होता है। यह सहसंयोजक बंध से भी कमजोर होता है। हाइड्रोजन बंध केवल फ्लोरीन, ऑक्सीजन और नाइट्रोजन के यौगिकों में पाया जाता है।
ऑक्सीकरण और अपचयन
- ऑक्सीकरण – जब किसी पदार्थ में विद्युत ऋणात्मकता बढ़ती है, धनात्मक आवेश बढ़ता है या इलेक्ट्रॉनों का निष्कर्षण होता है, तो उसे ऑक्सीकरण कहते हैं। उदाहरण— Na → Na⁺ + e⁻ (ऑक्सीकरण)
- अपचयन – जब किसी पदार्थ में विद्युत धनात्मकता बढ़ती है, धनात्मक आवेश कम होता है या इलेक्ट्रॉनों का ग्रहण होता है, तो उसे अपचयन कहते हैं। उदाहरण— Cu²⁺ + 2e⁻ → Cu (अपचयन)
- रेडॉक्स अभिक्रिया – ऑक्सीकरण और अपचयन की प्रक्रियाएँ हमेशा साथ-साथ होती हैं। जब एक पदार्थ इलेक्ट्रॉन खोता है और दूसरा पदार्थ इलेक्ट्रॉन ग्रहण करता है, तो ऐसी अभिक्रिया को रेडॉक्स अभिक्रिया कहते हैं।
अम्ल, क्षार और लवण
अम्ल
- अरहेनियस के अनुसार: अम्ल वह पदार्थ है जो जलीय विलयन में H⁺ आयन देता है।
- ब्रॉन्स्टेड–लॉरी सिद्धांत के अनुसार: अम्ल वह पदार्थ है जो किसी अन्य पदार्थ को प्रोटॉन (H⁺) प्रदान करने की क्षमता रखता है।
- लुईस के इलेक्ट्रॉनिक सिद्धांत के अनुसार: अम्ल वह पदार्थ है जो इलेक्ट्रॉनों के एकाकी युग्म को स्वीकार करने की प्रवृत्ति रखता है।
- अम्ल का स्वाद खट्टा होता है। अम्ल का जलीय विलयन नीले लिटमस पत्र को लाल कर देता है।
कुछ प्राकृतिक अम्ल/ क्षार
| प्राकृतिक अम्ल / क्षार | उपस्थिति |
| मैलिक अम्ल | सेब |
| एसिटिक अम्ल | सिरका |
| फॉर्मिक अम्ल | चींटी का डंक |
| सिट्रिक अम्ल | खट्टे फल नारंगी नींबू |
| लैक्टिक अम्ल | दही |
| ऑक्सैलिक अम्ल | पालक टमाटर |
| एस्कॉर्बिक अम्ल | विटामिन सी, आंवला खट्टे फल |
| टार्टरिक अम्ल | अंगूर कच्चे आम इमली |
| मेथेनोइक अम्ल | चींटी का डंक, बिछुआ का डंक |
| कैल्शियम हाइड्रॉक्साइड | चूने का पानी |
| मैग्नीशियम हाइड्रॉक्साइड | मिल्क ऑफ मैग्नीशिया |
अम्लों के उपयोग
- खाद्य पदार्थों में: दही (लैक्टिक अम्ल), सिरका और अचार (एसिटिक अम्ल), सोडा वाटर और सॉफ्ट ड्रिंक (कार्बोनिक अम्ल), अंगूर (टार्टरिक अम्ल), सेब (मैलिक अम्ल), नींबू और संतरा (सिट्रिक अम्ल)।
- नोट: टार्टरिक अम्ल का उपयोग बेकिंग पाउडर बनाने में किया जाता है।
- हाइड्रोक्लोरिक अम्ल (HCl) भोजन के पाचन में सहायक होता है।
- नाइट्रिक अम्ल (HNO₃) का उपयोग सोने और चाँदी के आभूषणों के निर्माण में किया जाता है।
- सल्फ्यूरिक अम्ल (H₂SO₄) और नाइट्रिक अम्ल (HNO₃) का उपयोग लोहे और इस्पात से जंग साफ करने में किया जाता है।
- नोट: कपड़ों से जंग के दाग हटाने के लिए ऑक्सैलिक अम्ल का उपयोग किया जाता है। इसका उपयोग फोटोग्राफी में भी किया जाता है।
- चींटी के काटने पर शरीर में फॉर्मिक अम्ल प्रवेश करता है। इसे निष्क्रिय करने के लिए त्वचा पर बेकिंग सोडा लगाया जाता है।
एक्वा रेजिया
- यह सांद्र हाइड्रोक्लोरिक अम्ल और सांद्र नाइट्रिक अम्ल का 3 : 1 अनुपात में बना मिश्रण होता है। इसमें सोना और प्लेटिनम को घोलने की क्षमता होती है।
- नोट : हाइड्रोक्लोरिक अम्ल (HCl) को म्यूरिएटिक एसिड तथा सल्फ्यूरिक अम्ल (H₂SO₄) को ऑयल ऑफ विट्रिऑल कहा जाता है। HCl एक खनिज अम्ल है।
क्षार
- क्षार वह यौगिक है जो किसी अम्ल के साथ अभिक्रिया करके लवण और जल बनाता है।
- ब्रॉन्स्टेड–लॉरी सिद्धांत के अनुसार: क्षार वह पदार्थ है जो प्रोटॉन (H⁺) को ग्रहण करने की क्षमता रखता है।
- लुईस के इलेक्ट्रॉनिक सिद्धांत के अनुसार: क्षार वह पदार्थ है जो इलेक्ट्रॉनों का एकाकी युग्म प्रदान कर सकता है।
कुछ महत्वपूर्ण क्षारों के उपयोग
- कैल्शियम हाइड्रॉक्साइड [Ca(OH)₂]: घरों की सफेदी करने में, मोर्टार और प्लास्टर बनाने में, ब्लीचिंग पाउडर के निर्माण में।
- कास्टिक सोडा या सोडियम हाइड्रोक्साइड (NaOH): साबुन बनाने में, पेट्रोलियम शोधन में, दवाइयां बनाने में, कपड़ा और कागज उद्योग में, नालियों की सफाई में।
- मिल्क ऑफ मैग्नीशिया या मैग्नीशियम हाइड्रॉक्साइड [Mg(OH)₂]: की अम्लता को कम करने के लिए उपयोग किया जाता है।
- नोट: यातायात पुलिस द्वारा नशे की जांच के लिए किया जाने वाला श्वास परीक्षण (Breath test) अम्ल–क्षार अभिक्रिया के सिद्धांत पर आधारित होता है।
| सूचक | अम्लीय | क्षारीय |
| लिटमस पेपर | नीले लिटमस को लाल कर देता है | लाल लिटमस को नीला कर देता है |
| फीनॉलफ्थेलिन | रंगहीन | गुलाबी रंग |
| मिथाइल नारंगी | लाल रंग | पीला रंग |
| गुड़हल/चाइना रोज | गहरे गुलाबी | हरा रंग |
संयुग्मी अम्ल और क्षार
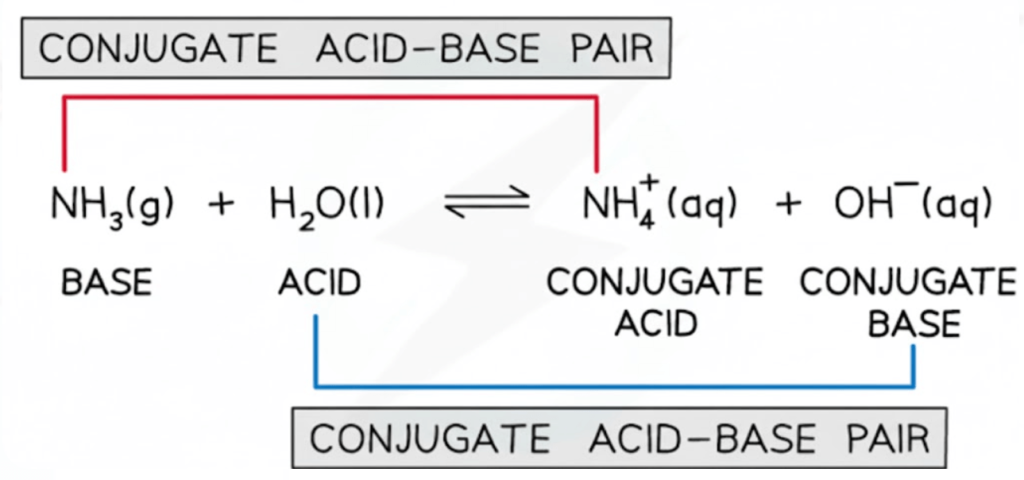
- ब्रॉन्स्टेड–लॉरी सिद्धांत के अनुसार जब कोई क्षार एक प्रोटॉन (H⁺) को ग्रहण करता है तो संयुग्मी अम्ल बनता है। और जब कोई अम्ल एक प्रोटॉन (H⁺) दान करता है, तो उसके बाद जो पदार्थ बचता है उसे संयुग्मी क्षार कहते हैं।
- संयुग्मी अम्ल और संयुग्मी क्षार संयुग्मी अम्ल–क्षार युग्म के रूप में पाए जाते हैं। इनमें केवल एक प्रोटॉन (H⁺) का अंतर होता है। इस कारण अम्ल–क्षार अभिक्रियाएँ प्रतिवर्ती हो सकती हैं, जहाँ अम्ल अपना प्रोटॉन देकर संयुग्मी क्षार बन जाता है और क्षार प्रोटॉन ग्रहण करके संयुग्मी अम्ल बन जाता है।
संयुग्मी क्षार:
- वह पदार्थ जो किसी अम्ल द्वारा प्रोटॉन (H⁺) देने के बाद शेष रह जाता है, संयुग्मी क्षार कहलाता है।
- निर्माण: अम्ल → संयुग्मी क्षार + H⁺
- उदाहरण: HCl → Cl⁻ + H⁺
- यहाँ Cl⁻, HCl का संयुग्मी क्षार है।
संयुग्मी अम्ल:
- वह पदार्थ जो किसी क्षार द्वारा प्रोटॉन (H⁺) ग्रहण करने पर बनता है, संयुग्मी अम्ल कहलाता है।
- निर्माण: क्षार + H⁺ → संयुग्मी अम्ल
- उदाहरण: NH₃ + H⁺ → NH₄⁺
- यहाँ NH₄⁺, NH₃ का संयुग्मी अम्ल है।
लवण
- लवण वह पदार्थ है जो अम्ल और क्षार की अभिक्रिया के फलस्वरूप जल के साथ बनता है। उदाहरण— NaOH + HCl → NaCl + H₂O
कुछ महत्वपूर्ण लवणों के उपयोग
- साधारण नमक या सोडियम क्लोराइड(NaCl) : खाने के नमक के रूप में, अचार के संरक्षण में।
- बेकिंग सोडा या सोडियम बाइकार्बोनेट (NaHCO₃): पेट की अम्लता कम करने में, अग्निशामक यंत्रों में।
- वॉशिंग सोडा या सोडियम कार्बोनेट (Na₂CO₃·10H₂O): कपड़े धोने में।
- कास्टिक सोडा या सोडियम हाइड्रोक्साइड (NaOH): साबुन बनाने में।
- पोटैशियम नाइट्रेट (KNO₃): पटाखे बनाने में।
pH स्केल
- किसी विलयन की अम्लीयता या क्षारीयता को व्यक्त करने के लिए pH स्केल का उपयोग किया जाता है। pH = –log [H⁺]
- किसी विलयन में हाइड्रोजन आयनों (H⁺) की सांद्रता जितनी अधिक होगी, उस विलयन का pH मान उतना ही कम होगा।
- pH स्केल को सोरेनसेन ने 1909 में दिया था।
सामान्य द्रवों के pH मान
| द्रव | pH | द्रव | pH |
| नींबू का रस | 2.5 | रक्त | 7.4 |
| वाइन | 2.8 | समुद्री जल | 8.5 |
| सेब का रस | 3 | टूथपेस्ट | 9 |
| सिरका | 3 | मिल्क ऑफ मैग्नेशिया | 10.5 |
| मूत्र | 4.8 | दूध | 6.5 |
| कॉफी | 5 | शुद्ध जल | 7 |
| लार | 6.5 |
pH के आधार पर विलयन की प्रकृति –
- यदि किसी विलयन का pH मान 7 से कम होता है, तो वह अम्लीय होता है।
- यदि किसी विलयन का pH मान 7 से अधिक होता है, तो वह क्षारीय होता है।
- मानव शरीर सामान्य रूप से 7.0 से 7.8 के pH सीमा में ठीक प्रकार से कार्य करता है। जीवित जीव केवल सीमित pH सीमा में ही जीवित रह सकते हैं।
- जब वर्षा के पानी का pH मान 5.6 से कम हो जाता है, तो उसे अम्लीय वर्षा कहा जाता है।
- pH मान में परिवर्तन के कारण दाँतों का क्षय शुरू हो जाता है। जब मुँह का pH मान 5.5 से कम हो जाता है, तब दाँतों का इनेमल क्षतिग्रस्त होने लगता है।
- दाँतों का इनेमल कैल्शियम फॉस्फेट से बना होता है। यह सामान्यतः पानी में नहीं घुलता, लेकिन जब मुँह का pH 5.5 से नीचे चला जाता है तो यह धीरे-धीरे क्षतिग्रस्त होने लगता है।
दैनिक जीवन में pH का महत्व
- पौधे और पशु केवल pH के संकीर्ण दायरे में ही जीवित रह सकते हैं। सामान्यतः मनुष्य और पशुओं का शरीर 7 से 7.8 के pH सीमा में कार्य करता है।
- मिट्टी के pH मान में परिवर्तन होने से मिट्टी अनुपजाऊ हो सकती है।
- अपच होने पर पेट में हाइड्रोक्लोरिक अम्ल (HCl) की मात्रा बढ़ जाती है, जिससे दर्द और जलन होता है। इसका उपचार एंटासिड से किया जाता है।
- जब मधुमक्खी किसी व्यक्ति को डंक मारती है, तो वह त्वचा में फॉर्मिक अम्ल छोड़ती है। इसे कम करने के लिए बेकिंग सोडा जैसे हल्के क्षार का उपयोग किया जाता है।
- दूध में उपस्थित सूक्ष्मजीव और यीस्ट लैक्टिक अम्ल बनाते हैं, जिससे दूध में अम्लता बढ़ जाती है। बेकिंग सोडा लैक्टिक अम्ल के बनने को रोकता है, इसलिए कभी-कभी दूध विक्रेता दूध में बेकिंग सोडा मिला देते हैं।
- केले के पत्ते क्षारीय प्रकृति के होते हैं और यीस्ट की वृद्धि को रोकते हैं, इसलिए दूध के बर्तनों में केले के पत्ते रखे जाते हैं।
विलयन
- विलयन दो या दो से अधिक पदार्थों का समांगी मिश्रण होता है, जिसमें किसी निश्चित तापमान पर विलेय और विलायक की सापेक्ष मात्रा एक निश्चित सीमा के भीतर बदल सकती है।
विक्षेपण
- जब किसी एक पदार्थ के कण (परमाणु, अणु या आयन) दूसरे पदार्थ के कणों के बीच समान रूप से फैल जाते हैं, तो इस प्रक्रिया को विक्षेपण कहते हैं।
- पहले पदार्थ को विक्षेपित अवस्था तथा दूसरे पदार्थ को विक्षेपण माध्यम कहते हैं।
- विक्षेपण के आधार पर पदार्थ तीन प्रकार के होते हैं—
- निलंबन –इसमें प्रकीर्णित कणों का आकार लगभग 10⁻³ सेमी से 10⁻⁴ सेमी या उससे अधिक होता है। ये कण नंगी आँखों से देखे जा सकते हैं। इनके कण फिल्टर पेपर से नहीं गुजरते और स्थिर रखने पर नीचे बैठने की प्रवृत्ति रखते हैं। उदाहरण— नदी का गंदला पानी, वायु में धुआँ आदि।
- कोलॉइड – इसमें प्रकीर्णित कणों का आकार लगभग 10⁻⁵ सेमी से 10⁻⁷ सेमी के बीच होता है। ये कण फिल्टर पेपर से गुजर सकते हैं, लेकिन जंतु झिल्ली से नहीं गुजरते। इनके कणों के नीचे बैठने की प्रवृत्ति निलंबन से कम होती है। उदाहरण— दूध, रक्त, कोहरा, स्याही आदि।
- इमल्शन – वह कोलॉइड जिसमें विक्षेपित अवस्था और विक्षेपित माध्यम दोनों द्रव होते हैं, उसे इमल्शन कहते हैं। इमल्शन बनने की प्रक्रिया को इमल्सीकरण कहते हैं। दूध एक प्राकृतिक इमल्शन है, जबकि मक्खन एक कृत्रिम इमल्शन है। मक्खन में तेल में जल का विक्षेपण होता है, जो इमल्शन का एक उदाहरण है। बड़े पैमाने पर इमल्सीकरण के लिए साबुन और डिटर्जेंट जैसे इमल्सीकारक का उपयोग किया जाता है। कपड़ों की सफाई में भी इमल्सीकरण की प्रक्रिया का उपयोग होता है। इमल्सीकारक पदार्थों का उपयोग दवाइयों के निर्माण में भी किया जाता है।
कोलॉइड के विभिन्न प्रकार
| विक्षेपण प्रावस्था | विक्षेपण माध्यम | कोलॉइड | उदाहरण |
| द्रव | गैस | एरोसोल | कोहरा, बादल, धुंध |
| ठोस | गैस | एरोसोल | धुआँ, वाहनों का धुआँ |
| गैस | द्रव | फोम | शेविंग क्रीम |
| द्रव | द्रव | इमल्शन | दूध, फेस क्रीम |
| ठोस | द्रव | सोल | मिल्क ऑफ मैग्नेशिया, कीचड़ |
| गैस | ठोस | फोम | फोम, रबर, स्पंज, प्यूमिस |
| द्रव | ठोस | जेल | जेली, पनीर, मक्खन |
| ठोस | ठोस | ठोस सोल | रंगीन रत्न, दूधिया काँच |
ब्राउनियन गति
- कोलॉइडी विलयन के कणों की टेढ़ी-मेढ़ी (जिग-जैग) गति को ब्राउनियन गति कहते हैं।
- यह गति कणों के स्वभाव पर निर्भर नहीं करती। कण जितने छोटे होते हैं और प्रकीर्णन माध्यम जितना हल्का होता है, यह गति उतनी ही तेज होती है।
टिंडल प्रभाव
- जब प्रकाश की तेज किरण किसी कोलॉइडी विलयन से होकर गुजरती है और उसे सूक्ष्मदर्शी की सहायता से समकोण पर देखा जाता है, तो कोलॉइडी कण अंधेरी पृष्ठभूमि पर छोटे-छोटे चमकते बिंदुओं के रूप में दिखाई देते हैं। इस घटना को टिंडल प्रभाव कहते हैं। यह प्रभाव प्रकाश के प्रकीर्णन के कारण होता है।
कार्बन और उसके यौगिक
- कार्बन एक तत्व है जिसका परमाणु क्रमांक 6 है। यह आधुनिक आवर्त सारणी के समूह IVA (समूह 14) में स्थित है।
- केकुले ने बताया कि कार्बन की संयोजकता चार होती है। इसी कारण कार्बन के यौगिकों में शृंखलन और संरचनात्मक विविधता पाई जाती है।
- अपररूपता – वे पदार्थ जिनके रासायनिक गुण समान होते हैं लेकिन भौतिक गुण भिन्न होते हैं, उन्हें अपररूप कहते हैं। इस घटना को अपररूपता कहते हैं।
- कार्बन के मुख्य अपररूप :
हीरा
- हीरा प्रकृति में पाया जाने वाला सबसे कठोर पदार्थ है। यह ऊष्मा और विद्युत का अच्छा चालक होता है।
- यह किसी भी द्रव में घुलता नहीं है और अम्ल तथा क्षार का इस पर कोई प्रभाव नहीं पड़ता। इसका सापेक्ष घनत्व 3.52 होता है। इसका अपवर्तनांक 2.417 होता है, इसलिए इसमें अधिक चमक होती है।
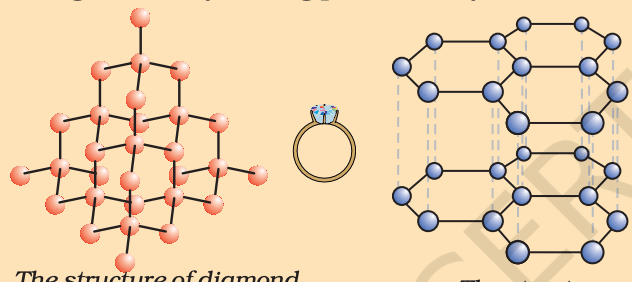
- हीरे में प्रत्येक कार्बन परमाणु चार अन्य कार्बन परमाणुओं से जुड़कर टेट्राहेड्रल संरचना बनाता है, जिससे त्रिविमीय संरचना बनती है।
- एक्स-किरणों के संपर्क में आने पर इसमें हरा फ्लोरेसेंस दिखाई देता है। शुद्ध हीरा पारदर्शी और रंगहीन होता है। इसका उपयोग काँच काटने में किया जाता है।
ग्रेफाइट
- ग्रेफाइट विद्युत का अच्छा चालक होता है। इसका सापेक्ष घनत्व 2.2 होता है।
- जब इसे कागज पर रगड़ा जाता है तो यह काला निशान छोड़ता है, इसलिए इसे ब्लैक लेड भी कहा जाता है।
- ग्रेफाइट में प्रत्येक कार्बन परमाणु तीन अन्य कार्बन परमाणुओं से जुड़कर षट्कोणीय संरचना बनाता है।
- हीरे में कार्बन sp³ संकरण अवस्था में होता है, जबकि ग्रेफाइट में कार्बन sp² संकरण अवस्था में होता है।
- हीरा ऊष्मा का अच्छा चालक होता है, जबकि ग्रेफाइट ऊष्मा और विद्युत दोनों का अच्छा चालक होता है।
बहुलकीकरण
- जब किसी एक ही यौगिक के दो या दो से अधिक अणु आपस में जुड़कर एक बड़ा अणु बनाते हैं, तो इस प्रक्रिया को बहुलकीकरण कहते हैं।
- इस प्रक्रिया में भाग लेने वाले सरल अणु को एकलक (मोनोमर) कहा जाता है और बनने वाले बड़े अणु को बहुलक (पॉलिमर) कहते हैं।
- प्राकृतिक बहुलकों के उदाहरण: स्टार्च और सेल्यूलोज।
- प्लास्टिक कृत्रिम बहुलक का एक उदाहरण है।
| थर्मोप्लास्टिक बहुलक | थर्मोसेटिंग प्लास्टिक बहुलक |
| ये प्लास्टिक गरम करने पर नरम हो जाते हैं और ठंडा करने पर फिर से कठोर हो जाते हैं। यह प्रक्रिया कई बार दोहराई जा सकती है। इनके अणुओं की संरचना लंबी रैखिक शृंखलाओं की होती है, इसलिए गरम करने पर ये आसानी से नरम हो जाते हैं। उदाहरण : पॉलीएथीन, पॉलीस्टाइरीन, पॉलीविनाइल क्लोराइड, टेफ्लॉन | ये प्लास्टिक गरम करने पर केवल एक बार नरम होते हैं और फिर स्थायी रूप से कठोर हो जाते हैं। एक बार कठोर हो जाने के बाद इन्हें दोबारा गरम करके नरम नहीं किया जा सकता। इसलिए इन्हें ऊष्मा-कठोर-बहुलक कहा जाता है। उदाहरण – मेलामाइन , बैकेलाइट , यूरिया |
नोट :
- पॉलीथीन का उपयोग विद्युत तारों की कोटिंग और पैकिंग सामग्री बनाने में किया जाता है।
- पॉलीविनाइल क्लोराइड का उपयोग रेनकोट बनाने में किया जाता है।
- पॉलीस्टाइरीन का उपयोग अम्ल के पात्र और पैकिंग बॉक्स बनाने में किया जाता है।
- बैकेलाइट का उपयोग रेडियो, टेलीविजन के केस, बाल्टी आदि बनाने में किया जाता है।
- टेफ्लॉन का उपयोग नॉन-स्टिक बर्तन बनाने में किया जाता है।
- मेलामाइन प्लास्टिक की कोटिंग करके अग्निरोधी कपड़े बनाए जाते हैं।
रबर
रबर दो प्रकार का होता है—
- प्राकृतिक रबर – यह आइसोप्रीन का बहुलक होता है और लचीला होता है।
- वल्कनीकरण – प्राकृतिक रबर को गंधक (सल्फर) के साथ गरम करने की प्रक्रिया को वल्कनीकरण कहते हैं।वल्कनीकरण के बाद रबर निश्चित आकार और अधिक मजबूती प्राप्त कर लेता है। इसलिए वल्कनीकृत रबर का उपयोग दस्ताने और रबर बैंड बनाने में किया जाता है। रबर के वल्कनीकरण की खोज चार्ल्स गुडईयर ने की थी। टायर बनाने के लिए रबर में लगभग 5% गंधक का उपयोग किया जाता है।
- कृत्रिम रबर – कृत्रिम रबर ब्यूटाडीन , स्टाइरीन और आइसोप्रीन के बहुलकीकरण से प्राप्त होता है।
रेशे
- वे श्रृंखलाकार ठोस पदार्थ जिनकी लंबाई उनकी चौड़ाई से सैकड़ों या हजारों गुना अधिक होती है, उन्हें रेशे कहते हैं।
- रेशों का वर्गीकरण
1. उत्पत्ति के आधार पर
- प्राकृतिक रेशे → ये रेशे प्रत्यक्ष रूप से पौधों या पशुओं से प्राप्त होते हैं।
- पादप रेशे → ये अधिकतर सेलुलोज (Cellulose) से बने होते हैं। उदाहरण— कपास, जूट, फ्लैक्स, भांग, नारियल रेशा
- जन्तु रेशे → ये अधिकतर प्रोटीन से बने होते हैं। उदाहरण— ऊन, रेशम, अल्पाका, ऊँट के बाल
- कृत्रिम रेशे → ये रेशे कारखानों में पेट्रोलियम या रासायनिक पदार्थों से बनाए जाते हैं। उदाहरण— नायलॉन, पॉलिएस्टर, ऐक्रेलिक
- अर्ध-कृत्रिम / पुनर्जनित रेशे → ये प्राकृतिक सेलुलोज से बनाए जाते हैं, लेकिन रासायनिक प्रक्रिया से तैयार किए जाते हैं। उदाहरण— रेयॉन, मोडल, लाइयोसेल, एसीटेट
2. रासायनिक संरचना के आधार पर
- सेलुलोज आधारित रेशे → ये कार्बोहाइड्रेट आधारित होते हैं और पौधों या पुनर्जनित सेलुलोज से प्राप्त होते हैं।
- प्राकृतिक → कपास, जूट, फ्लैक्स, भांग, नारियल रेशा
- मानव निर्मित → रेयॉन, लाइयोसेल, एसीटेट
- गैर-सेलुलोज रेशे →
- पशु मूल (प्रोटीन आधारित) → ऊन, रेशम
- कृत्रिम मूल (पेट्रोकेमिकल आधारित) → नायलॉन, पॉलिएस्टर, ऐक्रेलिक
गैसों का व्यवहार
- बॉयल का नियम –स्थिर तापमान पर किसी गैस के निश्चित द्रव्यमान का आयतन उसके दाब के व्युत्क्रमानुपाती होता है।
- चार्ल्स का नियम – स्थिर दाब पर किसी गैस के निश्चित द्रव्यमान का आयतन उसके परम ताप के सीधे अनुपाती होता है। (परम ताप T = 273 + t°C)
- आवोग्रादो का नियम – समान ताप और दाब पर सभी गैसों के समान आयतन में अणुओं की संख्या समान होती है। मानक ताप और दाब पर किसी भी गैस के एक ग्राम-अणु का आयतन 22.4 लीटर होता है और 22.4 लीटर में 6.022 × 10²³ अणु होते हैं। गैस समीकरण – PV = nRT, जहाँ R गैस स्थिरांक है।
- गैसों का विसरण – वह प्राकृतिक प्रक्रिया जिसमें गैसें आपस में संपर्क में रहते हुए स्वतः एक-दूसरे में मिल जाती हैं, उसे विसरण कहते हैं।
गैसों के उपयोग
- एल.पी.जी. (LPG) का मुख्य घटक ब्यूटेन होता है।
- कोयला खानों में फायर-डैम्प अर्थात मीथेन गैस वायु के साथ अधिक मात्रा में पाई जाती है।
- ब्यूटेन गैस का उपयोग मुख्य रूप से सिगरेट लाइटर में किया जाता है।
- रेफ्रिजरेंट गैस सामान्यतः डाइक्लोरो और डाइफ्लोरो यौगिकों के मिश्रण से बनी होती है।
- मस्टर्ड गैस का उपयोग प्रथम विश्व युद्ध में हथियार के रूप में किया गया था।
- एथिलीन का उपयोग फलों को कृत्रिम रूप से पकाने के लिए किया जाता है।
- जब कैल्शियम कार्बाइड (CaC₂) की पानी के साथ अभिक्रिया होती है, तो एसीटिलीन गैस बनती है।
नाइट्रोजन और द्रव नाइट्रोजन –
- डांस फ्लोर पर धुएँ जैसा प्रभाव बनाने के लिए उपयोग किया जाता है।
- क्रायोप्रिज़र्वेशन में— जैसे बैल के वीर्य, जीवित कोशिकाओं और ऊतकों को सुरक्षित रखने के लिए।
- खाद्य पदार्थों की पैकेजिंग (जैसे चिप्स के पैकेट) में निष्क्रिय वातावरण बनाने के लिए।
निष्क्रिय गैसें / नोबल गैसें
- क्रिप्टॉन – फोटोग्राफिक फ्लैश लैम्प में उपयोग होता है।
- जेनॉन – उच्च तीव्रता वाले लैम्प में उपयोग होता है।
- आर्गन – बल्ब और ट्यूबलाइट में, ऐतिहासिक दस्तावेजों (जैसे भारत का संविधान) को सुरक्षित रखने में, खाद्य पदार्थों के संरक्षण में।
- हीलियम – ऑक्सीजन के साथ मिलाकर कृत्रिम श्वसन में (अस्थमा रोगियों, गोताखोरों और अंतरिक्ष यात्रियों के लिए), विमान के टायर और गुब्बारे भरने में।
- नियॉन – फ्लोरोसेंट ट्यूब और वैक्यूम ट्यूब में, विज्ञापन साइनबोर्ड में लाल रंग की रोशनी देने के लिए।
विशेष गैसें
- आँसू गैस (CCl₃NO₂ – क्लोरोपिक्रिन) – भीड़ को नियंत्रित करने के लिए पुलिस द्वारा उपयोग की जाती है।
- लाफिंग गैस (N₂O) – हल्का निश्चेतक, जिसका उपयोग दंत चिकित्सा और दर्द कम करने में किया जाता है।
- एसिटिलीन (C₂H₂) – ऑक्सी-एसीटिलीन वेल्डिंग में, फलों को जल्दी पकाने के लिए।
- एथिलीन (C₂H₄) – एक पादप हार्मोन है, जिसका उपयोग फलों के कृत्रिम पकने में किया जाता है।
गैसीय ईंधन
- प्राकृतिक गैस – यह पेट्रोलियम के कुओं से प्राप्त होती है। इसमें लगभग 95% हाइड्रोकार्बन होते हैं, जिनमें से लगभग 80% मीथेन होता है।
- द्रवीकृत पेट्रोलियम गैस (LPG)
- दाब के प्रभाव से द्रव में परिवर्तित पेट्रोलियम गैस को द्रवीकृत पेट्रोलियम गैस (LPG) कहते हैं।
- यह मुख्य रूप से ब्यूटेन और आइसोब्यूटेन का मिश्रण होती है, जिसमें थोड़ी मात्रा में प्रोपेन भी होता है। इसे दाब के तहत आसानी से द्रव रूप में संपीड़ित करके लोहे के सिलेंडरों में संग्रहित किया जाता है।
- इसका उपयोग घरेलू ईंधन के रूप में किया जाता है।
- LPG सिलेंडर से गैस के रिसाव पर आने वाली दुर्गंध का कारण एथिल मरकैप्टन होता है।
- संपीड़ित प्राकृतिक गैस (CNG)
- बहुत अधिक दाब पर संपीडित प्राकृतिक गैस को CNG कहते हैं।
- इसमें मुख्य रूप से मीथेन (लगभग 95%) होता है, जो अपेक्षाकृत कम अभिक्रियाशील हाइड्रोकार्बन है और इसका दहन लगभग पूर्ण होता है।
- शेष लगभग 5% भाग में एथेन, प्रोपेन, ब्यूटेन, जलवाष्प तथा थोड़ी मात्रा में N₂, CO₂, H₂S आदि गैसें होती हैं।
- CNG का उपयोग आजकल बस, कार और तीन-पहिया वाहनों को चलाने के लिए ईंधन के रूप में किया जाता है, क्योंकि इसका दहन पूर्ण होता है और वातावरण में अजला कार्बन नहीं छोड़ता, जिससे वायु प्रदूषण कम होता है।
- बायोगैस (गोबर गैस) – गीले गोबर (पशु अपशिष्ट) के अपघटन से ज्वलनशील मीथेन गैस बनती है, जो वायु की उपस्थिति में अधिक दक्षता से जलती है। गौबर गैस संयंत्र से प्राप्त स्लरी का उपयोग जैविक खाद के रूप में किया जाता है। बायोगैस में मुख्यतः— मीथेन (लगभग 65%), कार्बन डाइऑक्साइड, हाइड्रोजन और अमोनिया होते हैं।
- भाप अंगार गैस (जल गैस) – यह कार्बन मोनोऑक्साइड (CO) और हाइड्रोजन (H₂) का मिश्रण होती है। अभिक्रिया: C + H₂O → CO + H₂ (भाप अंगार गैस)
- उत्पादक गैस – यह CO और N₂ का मिश्रण होती है। इसे कोक को सीमित वायु में जलाकर तैयार किया जाता है। यह सबसे सस्ता गैसीय ईंधन माना जाता है।
- कोल गैस – यह H₂, CH₄, CO तथा अन्य गैसों जैसे N₂, C₂H₄, O₂ आदि का मिश्रण होती है।
- ऑयल गैस – यह H₂, CH₄, C₂H₄, CO तथा अन्य गैसों जैसे CO₂ आदि का मिश्रण होती है।
- मार्श गैस – यह प्राकृतिक रूप से दलदली क्षेत्रों में बनती है। इसमें मुख्य रूप से मीथेन, हाइड्रोजन सल्फाइड और कार्बन डाइऑक्साइड होते हैं।
संक्षारण
- धातुओं की सतह पर वायु और नमी के प्रभाव से उनका धीरे-धीरे नष्ट होना संक्षारण कहलाता है।
- लोहे पर जंग लगना, तांबे पर हरी परत बनना और चाँदी पर काली परत बनना संक्षारण के उदाहरण हैं।
- लोहे में जंग लगने के लिए वायु में ऑक्सीजन और नमी दोनों का होना आवश्यक होता है। लोहे का जंग लगना रासायनिक परिवर्तन का उदाहरण है। जंग लगने पर लोहे का द्रव्यमान बढ़ जाता है। जंग लगने पर बनने वाला पदार्थ फेरिक ऑक्साइड (Fe₂O₃·xH₂O) होता है।
- पेंट करने, तेल या ग्रीस लगाने, यशदीकरण या जस्तीकरण (गैल्वनाइजेशन), क्रोमियम प्लेटिंग, एनोडाइजेशन या मिश्रधातु बनाने से लोहे को जंग से बचाया जा सकता है।
- नोट : लोहे और इस्पात को जंग से बचाने के लिए उन पर जिंक (जस्ता) की पतली परत चढ़ाने की विधि को यशदीकरण कहते हैं।
- तांबा वायु में उपस्थित नमी और कार्बन डाइऑक्साइड के साथ अभिक्रिया करता है, जिससे उसकी सतह की चमक धीरे-धीरे कम हो जाती है और उस पर हरी परत बन जाती है। यह हरा पदार्थ कॉपर कार्बोनेट होता है।
- शुद्ध तांबा लाल रंग की धातु होता है। मानव शरीर में तांबे की मात्रा बढ़ जाने पर एक रोग उत्पन्न होता है जिसे विल्सन रोग कहते हैं।
- जब चाँदी की वस्तुएँ कुछ दिनों तक खुली हवा में रखी रहती हैं, तो वे काली पड़ जाती हैं। चाँदी वायु में उपस्थित गंधक (सल्फर) के साथ अभिक्रिया करके सिल्वर सल्फाइड की परत बना लेती है, जिसके कारण यह परिवर्तन होता है।
धातुओं से संबंधित विभिन्न तथ्य
धातुओं में अपवाद
- पारा (Hg) – अधिकांश धातुएँ सामान्य ताप पर ठोस होती हैं, लेकिन पारा सामान्य ताप पर द्रव अवस्था में पाया जाता है।
- क्षार धातुएँ (Na, K आदि) – धातुएँ सामान्यतः कठोर होती हैं, लेकिन सोडियम और पोटैशियम जैसी धातुएँ नरम होती हैं और इन्हें चाकू से काटा जा सकता है।
- गैलियम (Ga) – अधिकांश धातुओं का गलनांक अधिक होता है, लेकिन गैलियम का गलनांक बहुत कम होता है।
अधातुओं में अपवाद
- ब्रोमीन (Br) – अधातुएँ सामान्यतः ठोस या गैस अवस्था में होती हैं, लेकिन ब्रोमीन सामान्य ताप पर द्रव अवस्था में पाया जाता है।
- आयोडीन (I) – अधातुएँ सामान्यतः चमकहीन होती हैं, लेकिन आयोडीन में धात्विक चमक पाई जाती है।
अन्य महत्वपूर्ण तथ्य
- पृथ्वी के केंद्र में निकेल की मात्रा सबसे अधिक पाई जाती है और उसके बाद लोहा दूसरा सबसे अधिक पाया जाने वाला धातु है।
- टंगस्टन फिलामेंट के ऑक्सीकरण को रोकने के लिए विद्युत बल्बों से वायु निकाल दी जाती है।
- न्यूट्रॉन को अवशोषित करने के गुण के कारण जिरकोनियम और बोरॉन का उपयोग नाभिकीय रिएक्टरों में किया जाता है।
- टिन सल्फाइड (SnS₂) को मोज़ेक गोल्ड कहा जाता है। इसका उपयोग पेंट बनाने में किया जाता है। यह टिन की अपररूपता का गुण दर्शाता है।
- सोडियम धातु को केरोसीन तेल में संग्रहित करके रखा जाता है।
- सोडियम का उपयोग सड़क प्रकाश व्यवस्था में किया जाता है, जो सड़क और यातायात प्रकाश के लिए लगाए जाते हैं।
- प्लास्टर ऑफ पेरिस जिप्सम से तैयार किया जाता है।
- चूने से पुती हुई दीवारें दो से तीन दिन तक चमकदार दिखाई देती हैं, क्योंकि उस पर कैल्शियम कार्बोनेट बन जाता है।
- पटाखों में हरा रंग बेरियम की उपस्थिति के कारण तथा गहरा लाल (क्रिमसन रेड) रंग स्ट्रॉन्शियम (Sr) की उपस्थिति के कारण उत्पन्न होता है।
- सोडियम आयन (Na⁺) तंत्रिका आवेगों के संचरण के लिए जिम्मेदार होते हैं। सोडियम आयन मुख्यतः रक्त प्लाज़्मा और अंतरकोशिकीय द्रव में पाए जाते हैं।
- पोटैशियम आयन (K⁺) कोशिकीय द्रव में अधिक मात्रा में पाए जाते हैं। ये एंजाइम सक्रियण तथा ग्लूकोज के ऑक्सीकरण से ATP के निर्माण में भाग लेते हैं।
- लिथियम सबसे हल्का धात्विक तत्व है। यह सबसे शक्तिशाली अपचायक है।
- सोना, प्लैटिनम और चाँदी को नोबल धातुएँ (Noble metals) कहा जाता है।
- धातुओं में सबसे अधिक घनत्व सोने (Au) का तथा उसके बाद चाँदी (Ag) का होता है।
- सोडियम परबोरेट का उपयोग कपड़े धोने और सफाई में किया जाता है।
- सबसे भारी धातु ऑस्मियम है, सबसे कठोर धातु क्रोमियम है और सबसे अधिक गलनांक वाली धातु टंगस्टन है।
- पोटैशियम कार्बोनेट (K₂CO₃) को पर्ल ऐश कहा जाता है।
- नाइक्रोम निकेल, क्रोमियम और लोहे की मिश्रधातु है। इलेक्ट्रिक हीटर की कुंडली नाइक्रोम से बनाई जाती है।
- ब्रिटानिया धातु एंटीमनी (Sb), ताँबा और टिन (Sn) की मिश्रधातु है। इसका उपयोग टेबलवेयर बनाने और चाँदी की परत चढ़ाने के आधार के रूप में किया जाता है।
- बैबिट धातु में 89% टिन, 9% एंटीमनी और 2% ताँबा होता है।
- एल्युमिनियम हाइड्रॉक्साइड का उपयोग अग्निरोधी और जलरोधक कपड़े बनाने में किया जाता है।
- कैल्शियम कार्बाइड पानी के साथ अभिक्रिया करके एसीटिलीन गैस बनाता है।
- पिटवाँ लोहा में कार्बन की मात्रा सबसे कम (0.12–0.25%) होती है, इसलिए यह अधिक तन्य और कठोर होता है।
- आयरन (III) ऑक्साइड (Fe₂O₃) और एल्युमिनियम की अभिक्रिया का उपयोग रेलवे ट्रैक और विद्युत खंभों की वेल्डिंग में किया जाता है, जिसे थर्माइट वेल्डिंग कहते हैं।
- सिल्वर क्लोराइड (AgCl) को हॉर्न सिल्वर कहा जाता है। इसका उपयोग फोटोग्राफिक पेपर में किया जाता है।
- सिल्वर नाइट्रेट (AgNO₃) का उपयोग अमिट स्याही बनाने में किया जाता है। चुनाव के समय इसे मतदाताओं की उँगलियों पर लगाया जाता है। यह सूर्य के प्रकाश में विघटित हो जाता है, इसलिए इसे रंगीन बोतलों में रखा जाता है।
- सिल्वर ब्रोमाइड (AgBr) का उपयोग फोटोग्राफी में किया जाता है।
- चाँदी हवा के संपर्क में आने पर काली हो जाती है, क्योंकि यह गंधक के साथ अभिक्रिया करके सिल्वर सल्फाइड (Ag₂S) बनाती है।
- सोने को कठोर बनाने के लिए उसमें ताँबा या चाँदी मिलाया जाता है। शुद्ध सोना 24 कैरेट का होता है, जबकि आभूषणों में 22 कैरेट सोना प्रयोग किया जाता है।
- आयरन पाइराइट (FeS₂) को ‘’मूर्खों का सोना’’ कहा जाता है।
- प्लैटिनम को “सफेद सोना” कहा जाता है।
- पारा को क्विक सिल्वर भी कहा जाता है। यह मुख्यतः सिनेबार से प्राप्त किया जाता है। पारे को लोहे के पात्रों में रखा जाता है क्योंकि यह लोहे के साथ अमलगम नहीं बनाता।
- विद्युत उपकरणों में प्रयुक्त फ्यूज तार सीसा और टिन की मिश्रधातु का बना होता है।
- ग्रीन विट्रिऑल – फेरस सल्फेट (FeSO₄·7H₂O)
- व्हाइट विट्रिऑल – जिंक सल्फेट (ZnSO₄·7H₂O)
- ब्लू विट्रिऑल – कॉपर सल्फेट (CuSO₄·5H₂O), इसे रोमन विट्रिऑल भी कहा जाता है।
- रेड विट्रिऑल – कोबाल्ट सल्फेट (CoSO₄·7H₂O)
- जिंक फॉस्फाइड का उपयोग फफूंदनाशी तथा चूहे मारने की दवा के रूप में किया जाता है।
- मैग्नीशियम कार्बोनेट टूथ पाउडर का प्रमुख घटक होता है।
- मैग्नीशियम (जला हुआ रूप) का उपयोग फ्लैश पाउडर और पटाखों में किया जाता है।
- प्याज और लहसुन की गंध विभिन्न सल्फर यौगिकों के कारण होती है।
- पोटैशियम ब्रोमाइड का उपयोग फोटोग्राफी में, मोनो-पोटैशियम टार्ट्रेट का उपयोग बेकरी में, पोटैशियम सल्फेट का उपयोग उर्वरक के रूप में तथा पोटैशियम नाइट्रेट का उपयोग बारूद में किया जाता है।
- मोती की रासायनिक संरचना कैल्शियम कार्बोनेट (CaCO₃) होती है।
- रूबी और नीलम में एल्युमिनियम ऑक्साइड (Al₂O₃) होता है, लेकिन रूबी का लाल रंग क्रोमियम ऑक्साइड के कारण होता है।ऽ
उपधातु
- उपधातु वे रासायनिक तत्व होते हैं जिनके गुण धातुओं और अधातुओं के बीच के होते हैं या जिनमें दोनों के गुणों का मिश्रण पाया जाता है।
आधुनिक आवर्त सारणी में कुल 7 उपधातुएँ होती हैं—
- बोरॉन (B), सिलिकॉन (Si), जर्मेनियम (Ge), आर्सेनिक (As), एंटीमनी (Sb), टेल्यूरियम (Te), पोलोनियम (Po)।
- सिलिकॉन और जर्मेनियम का उपयोग व्यापक रूप से अर्धचालक उद्योग में किया जाता है।
मृदु जल और कठोर जल
- वह जल जो साबुन के साथ आसानी से झाग बनाता है, मृदु जल कहलाता है।
- वह जल जो साबुन के साथ आसानी से झाग नहीं बनाता, कठोर जल कहलाता है।
- अस्थायी कठोरता – यह कैल्शियम और मैग्नीशियम के बाइकार्बोनेट की उपस्थिति के कारण होती है। इसे उबालकर दूर किया जा सकता है।
- स्थायी कठोरता – यह कैल्शियम और मैग्नीशियम के क्लोराइड तथा सल्फेट के कारण होती है। इसे निम्न विधियों से दूर किया जाता है—
- धावन सोडा विधि
- जियोलाइट विधि
मानव निर्मित पदार्थ
साबुन और डिटर्जेंट
- साबुन और डिटर्जेंट ऐसे पदार्थ हैं जिनका उपयोग कपड़े, बर्तन और शरीर की सफाई के लिए किया जाता है।
- जब साबुन या डिटर्जेंट को पानी में मिलाया जाता है, तो वे पानी का सतही तनाव कम कर देते हैं और झाग बनाते हैं, जिससे सफाई आसान हो जाती है।
साबुन
- साबुन लंबी श्रृंखला वाले वसीय अम्लों के सोडियम या पोटैशियम लवण होते हैं। ये वसीय अम्ल प्राकृतिक तेल और वसा जैसे वनस्पति तेल या पशु वसा से प्राप्त होते हैं।
- साबुन साबुनीकरण नामक प्रक्रिया द्वारा बनाया जाता है, जिसमें तेल या वसा की अभिक्रिया सोडियम हाइड्रॉक्साइड या पोटैशियम हाइड्रॉक्साइड के साथ कराई जाती है और इससे साबुन तथा ग्लिसरॉल बनते हैं।
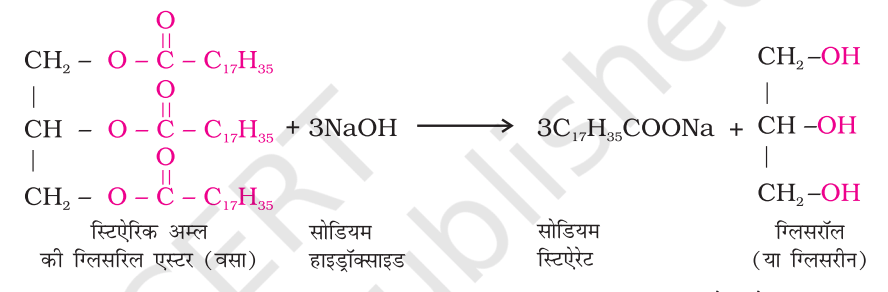
- साबुन मृदु जल में अच्छी तरह कार्य करता है, लेकिन कठोर जल में ठीक से कार्य नहीं करता, क्योंकि यह कैल्शियम और मैग्नीशियम आयनों के साथ अघुलनशील मैल बना देता है।
- उच्च वसीय अम्लों के सोडियम लवण को कठोर साबुन कहा जाता है। इसका उपयोग कपड़े धोने में किया जाता है।
- उच्च वसीय अम्लों के पोटैशियम लवण को मृदु साबुन कहा जाता है। इसका उपयोग मुख्य रूप से सफाई के लिए किया जाता है।
- साबुन सामान्यतः जैव अपघटनीय (Biodegradable) होते हैं, जबकि कई डिटर्जेंट (विशेषकर शाखित श्रृंखला वाले) जैव अपघटनीय नहीं होते।
- साबुन के अणु द्विप्रकृति होते हैं, अर्थात इनमें जलरागी (हाइड्रोफिलिक) और जलविरागी (हाइड्रोफोबिक) दोनों भाग होते हैं।
- मिसेल बनने की प्रक्रिया में—
- जलरागी भाग पानी के साथ क्रिया करता है।
- जलविरागी भाग तेल या चिकनाई के साथ क्रिया करता है।
डिटर्जेंट
- डिटर्जेंट कृत्रिम सफाई करने वाले पदार्थ होते हैं, जो रासायनिक पदार्थों से बनाए जाते हैं।
- ये सामान्यतः लंबी श्रृंखला वाले ऐल्किल सल्फेट या ऐल्किल बेंजीन सल्फोनेट के सोडियम लवण होते हैं।
- साबुन की तरह डिटर्जेंट में भी लंबी हाइड्रोकार्बन श्रृंखला और एक ध्रुवीय सिरा होता है, लेकिन साबुन के विपरीत डिटर्जेंट मृदु और कठोर दोनों प्रकार के जल में अच्छी तरह कार्य करते हैं।
- ऐसा इसलिए होता है क्योंकि कैल्शियम और मैग्नीशियम के साथ बनने वाले डिटर्जेंट के लवण पानी में घुलनशील होते हैं।
- ये Ca²⁺, Mg²⁺, Fe³⁺ आयनों वाले कठोर जल में भी झाग उत्पन्न करते हैं।
- उदाहरण: सोडियम ऐल्किल सल्फोनेट, सोडियम ऐल्किल बेंजीन सल्फोनेट आदि।
- नोट: जल में साबुन और डिटर्जेंट का झाग बनना मिसेल बनने के कारण होता है।
- साबुन सामान्यतः जैव अपघटनीय होते हैं और पर्यावरण को अधिक प्रदूषित नहीं करते, जबकि कई डिटर्जेंट अजैव अपघटनीय होते हैं और जल स्रोतों को प्रदूषित कर सकते हैं।
- फिर भी कठोर जल में कपड़े धोने के लिए डिटर्जेंट साबुन से अधिक प्रभावी होते हैं, इसलिए आजकल घरों में इनका अधिक उपयोग किया जाता है।
सफाई की प्रक्रिया
- साबुन और डिटर्जेंट दोनों के अणुओं के दो भाग होते हैं—
- जलरागी सिरा – यह पानी को आकर्षित करता है।
- जलविरागी सिरा – यह तेल और चिकनाई को आकर्षित करती है।
- जब साबुन या डिटर्जेंट को पानी में मिलाया जाता है, तो उनके अणु छोटे-छोटे समूह बनाते हैं जिन्हें मिसेल कहते हैं।
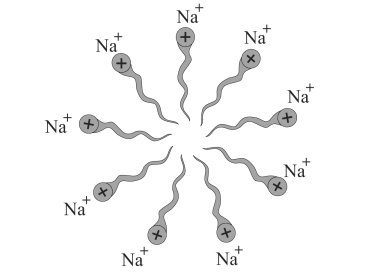
- तेल और गंदगी इन मिसेलों के अंदर फँस जाती है और धोने के दौरान पानी के साथ बहकर निकल जाती है।
उर्वरक
- वे रासायनिक पदार्थ जिन्हें मिट्टी में बाहर से मिलाया जाता है और जो फसल उत्पादन बढ़ाने में सहायक होते हैं, उन्हें उर्वरक कहते हैं।
- उर्वरक कई प्रकार के होते हैं—
- नाइट्रोजन उर्वरक: ये उर्वरक पौधों को मुख्य रूप से नाइट्रोजन प्रदान करते हैं।
- यूरिया (H₂NCONH₂) – इसमें लगभग 46% नाइट्रोजन होता है।
- अमोनियम सल्फेट [(NH₄)₂SO₄]
- कैल्शियम नाइट्रेट
- कैल्शियम सायनामाइड (CaCN₂)
- पोटैशियम उर्वरक –
- पोटैशियम क्लोराइड
- पोटैशियम नाइट्रेट
- पोटैशियम सल्फेट
- फॉस्फोरस उर्वरक –
- सुपर फॉस्फेट ऑफ लाइम
- फॉस्फेट रॉक
- फॉस्फोराइट
- सुपर फॉस्फेट में लगभग 16–20% P₂O₅ होता है।
कृत्रिम मधुरक
- प्राकृतिक मधुरक जैसे चीनी और गुड़ कैलोरी की मात्रा बढ़ाते हैं, इसलिए कई लोग कृत्रिम मधुरक को पसंद करते हैं।
- सैकरिन, जिसे बेंज़िमाइड भी कहा जाता है, पहला कृत्रिम मधुरक है। यह सुक्रोज से लगभग 550 गुना अधिक मीठा होता है। यह शरीर में उपापचय नहीं होता और अपरिवर्तित रूप में बाहर निकल जाता है। इसके उपयोग के बाद कड़वा और धात्विक स्वाद आता है। यह मधुमेह के रोगियों के लिए उपयोगी है।
- एस्पार्टेम सबसे अधिक उपयोग किया जाने वाला और सुरक्षित कृत्रिम मधुरक है। यह सुक्रोज से लगभग 100 गुना अधिक मीठा होता है।
| कृत्रिम मधुरक | गन्ना\शर्करा (सुक्रोज) की तुलना में मिठास मान |
| सैकरिन | 500 गुना |
| एलीटेम | 2000 गुना |
| सुक्रालोज़ | 600 गुना |
| एस्पार्टेम | 100 गुना |
- डल्सिन भी एक कृत्रिम मधुरक है। यह एस्पार्टेम से सस्ता है, लेकिन इसकी मिठास को नियंत्रित करना कठिन होने के कारण इसका उपयोग सीमित है।
- सुक्रालोज़ सुक्रोज का क्लोरीन युक्त व्युत्पन्न है। इसका स्वाद और मिठास चीनी के समान होता है। यह पकाने के तापमान पर स्थिर रहता है और कैलोरी नहीं देता।
खाद्य संरक्षक\खाद्य परिरक्षक
- संरक्षण\परिरक्षण: भोजन को खराब होने से बचाने और उसकी भंडारण अवधि बढ़ाने के लिए की जाने वाली प्रक्रिया को संरक्षण कहते हैं।
- संरक्षक\परिरक्षक: वे प्राकृतिक या रासायनिक पदार्थ जो भोजन में मिलाए जाते हैं ताकि सूक्ष्मजीवों की वृद्धि को रोका जा सके और भोजन खराब न हो। संरक्षक मुख्यतः—
- नमी कम करते हैं – सूक्ष्मजीवों को बढ़ने के लिए पानी की आवश्यकता होती है।
- सूक्ष्मजीवों की वृद्धि रोकते हैं – बैक्टीरिया, फफूंद और यीस्ट को नियंत्रित करते हैं।
- एंजाइम की क्रिया को नियंत्रित करते हैं – सड़ने या अधिक पकने की प्रक्रिया को धीमा करते हैं।
खाद्य संरक्षण की विधियाँ
- ऊष्मा उपचार — ऊष्मा हानिकारक सूक्ष्मजीवों को नष्ट कर देती है। उदाहरण— दूध का पाश्चुरीकरण, बोतलों का निर्जलीकरण।
- प्रशीतन एवं जमाना – कम तापमान पर एंजाइम और सूक्ष्मजीवों की क्रिया धीमी हो जाती है। उदाहरण— फल, सब्जियाँ और मांस को फ्रिज में रखना।
- सुखाना / निर्जलीकरण — इसमें भोजन से पानी की मात्रा निकाल दी जाती है, जिससे सूक्ष्मजीव नहीं बढ़ पाते। उदाहरण— सूखे फल, दूध पाउडर।
संरक्षकों का उपयोग
- प्राकृतिक संरक्षक : नमक, चीनी, मसाले, तेल, एसीटिक अम्ल (सिरका)
- उदाहरण: जैम (चीनी), अचार (नमक और तेल)।
- रासायनिक संरक्षक : इन्हें कम और सुरक्षित मात्रा में उपयोग किया जाता है।
- सोडियम बेंजोएट – केचप, फलों के रस और स्क्वैश में
- पोटैशियम मेटाबाइसुल्फाइट – स्क्वैश और जूस में (SO₂ उत्पन्न करता है जो संरक्षक का काम करता है)
- सोडियम मेटाबाइसुल्फाइट – भोजन के भूरा होने से रोकता है
- सॉर्बेट – दूध से बने उत्पादों के संरक्षण में
- पैराबेन्स – सॉफ्ट ड्रिंक्स में
- विकिरण द्वारा संरक्षण
- नियंत्रित परिस्थितियों में कोबाल्ट-60 से निकलने वाली गामा किरणों का उपयोग किया जाता है।
- इससे फलों, आलू, प्याज और मसालों की भंडारण अवधि बढ़ाई जाती है।
बाइंडर
- औषधि उद्योग में दवाई निर्माण की प्रक्रिया में बाइंडर महत्वपूर्ण भूमिका निभाते हैं। इनका उपयोग पाउडर मिश्रण की आपस में जुड़ने की क्षमता और प्लास्टिसिटी बढ़ाने के लिए किया जाता है। इससे दवाई निर्माण की प्रक्रिया आसान हो जाती है और निर्माण के दौरान दवाई के टूटने की संभावना कम हो जाती है।
- उदाहरण:
- प्राकृतिक बहुलक : अरेबिक गम, जिलेटिन, सोडियम एल्जिनेट, पुलुलन, स्टार्च, ट्रैगाकैंथ / ट्रैगेंट।
- अर्ध-कृत्रिम बहुलक : कार्बोक्सीमेथिल सेल्यूलोज सोडियम, डेक्सट्रिन, हाइड्रॉक्सीएथिल सेल्यूलोज, हाइड्रॉक्सीप्रोपाइल सेल्यूलोज, माल्टोडेक्सट्रिन, मिथाइल सेल्यूलोज।
- अन्य : पोविडोन, एथिल सेल्यूलोज।
रासायनिक और भौतिक परिवर्तन
| रासायनिक परिवर्तन | भौतिक परिवर्तन |
| वे परिवर्तन जिनमें एक या अधिक नए पदार्थ बनते हैं, रासायनिक परिवर्तन कहलाते हैं। | वे परिवर्तन जिनमें केवल भौतिक गुणों में परिवर्तन होता है और कोई नया पदार्थ नहीं बनता, भौतिक परिवर्तन कहलाते हैं।ये परिवर्तन प्रायः प्रतिवर्ती होते हैं। |
| उदाहरण | |
| प्रकाश संश्लेषण | पानी का उबलना |
| भोजन का पाचन | बर्फ का पिघलना |
| लोहे में जंग लगना | मोम या चीनी के टुकड़े का पिघलना |
| पत्तियों से खाद निर्माण | शुष्क बर्फ का उर्ध्वपातन |
| किसी पदार्थ का जलना | भाप का संघनन |
| फलों का पकना | रेत और पानी का मिश्रण |
| भोजन का खराब होना | लकड़ी काटना,सब्जी काटना |
| ओजोन का विघटन | चट्टानों का अपरदन |
| पटाखों का विस्फोट | एल्युमिनियम को पीटकर एल्युमीनियम फॉइल निर्माण |
| प्लास्टिक और दवाइयों का निर्माण | कागज़ के टुकड़े करना |
| उदासीनीकरण अभिक्रिया | |
